Ogniwo galwaniczne zrewolucjonizowało sposób, w jaki postrzegamy i wykorzystujemy energię elektryczną. Dzięki niemu zaczęto rozwijać nowe technologie, które zmieniły oblicze nauki i przemysłu. W tym artykule przyjrzymy się bliżej, jak działa ogniwo galwaniczne oraz jakie miało znaczenie dla współczesnego świata.
Najistotniejsze informacje:
- Alessandro Volta wynalazł ogniwo galwaniczne w 1800 roku, co zrewolucjonizowało naukę o elektryczności.
- Luigi Galvani, wcześniej, odkrył zjawiska elektryczne w tkankach zwierzęcych, co wpłynęło na badania Voltę.
- Ogniwo galwaniczne działa na zasadzie kontaktu różnych metali zanurzonych w elektrolicie, co generuje prąd elektryczny.
- Wynalazek Voltę stał się fundamentem dla dalszego rozwoju technologii, w tym baterii i urządzeń elektrycznych.
- Ogniwo galwaniczne miało kluczowy wpływ na rozwój nauki i przemysłu, umożliwiając nowe odkrycia i innowacje.
Kto wynalazł ogniwo galwaniczne i jego znaczenie dla nauki?
Pierwsze ogniwo galwaniczne wynalazł włoski uczony Alessandro Volta w 1800 roku. To odkrycie miało ogromne znaczenie dla rozwoju nauki i technologii. Volta, korzystając z wcześniejszych badań Luigi Galvaniego, zauważył, że prąd elektryczny powstaje w wyniku kontaktu różnych metali zanurzonych w elektrolicie. Jego wynalazek, znany jako „stos Volty”, zrewolucjonizował sposób, w jaki postrzegamy elektryczność.
Ogniwo galwaniczne nie tylko przyczyniło się do rozwoju teorii elektryczności, ale także otworzyło drzwi do dalszych badań w tej dziedzinie. Dzięki niemu powstały nowe technologie, które zmieniły oblicze przemysłu i codziennego życia. Odkrycie Voltę stało się fundamentem dla późniejszych innowacji, takich jak baterie i różne urządzenia elektryczne, które są kluczowe w dzisiejszym świecie.
Alessandro Volta: życie i dokonania w dziedzinie elektryczności
Alessandro Volta urodził się w 1745 roku w Como, we Włoszech. Był jednym z pierwszych naukowców, którzy systematycznie badali zjawiska elektryczne. Jego prace nad elektrycznością zaowocowały nie tylko wynalezieniem ogniwa galwanicznego, ale także stworzeniem pojęcia napięcia elektrycznego, które jest podstawą współczesnej elektroenergetyki. W 1800 roku Volta zaprezentował swoje odkrycie, które szybko zyskało uznanie wśród naukowców i wynalazców.
W ciągu swojej kariery Volta otrzymał wiele wyróżnień za swoje osiągnięcia. Jego wkład w rozwój nauki był nieoceniony. Volta był także profesorem na Uniwersytecie w Pawii, gdzie uczył przyszłe pokolenia naukowców. Jego prace miały wpływ na wielu badaczy, a jego nazwisko do dziś jest związane z jednostką napięcia elektrycznego – wolt.
Luigi Galvani: odkrycia, które wpłynęły na Volta
Luigi Galvani, włoski lekarz i fizyk, jest znany przede wszystkim z odkrycia zjawiska bioelektryczności. W 1786 roku przeprowadził eksperymenty na żabich nogach, które wykazały, że tkanki zwierzęce reagują na prąd elektryczny. Galvani zauważył, że kiedy do mięśni nogi żaby podłączono różne metale, występowały skurcze, co sugerowało istnienie „elektryczności zwierzęcej”. Te odkrycia stały się fundamentem dla dalszych badań nad elektrycznością i miały ogromny wpływ na rozwój teorii elektryczności.
Wpływ odkryć Galvaniego na pracę Alessandra Volt był nieoceniony. Volta, opierając się na wcześniejszych badaniach Galvaniego, zrozumiał, że prąd elektryczny można generować nie tylko w tkankach zwierzęcych, ale również poprzez kontakt różnych metali. To spostrzeżenie doprowadziło go do skonstruowania pierwszego ogniwa galwanicznego, które zrewolucjonizowało nasze podejście do elektryczności. Dzięki Galvaniemu, Volta mógł rozwijać swoje pomysły, co zaowocowało wynalezieniem „stosu Volt” i dalszymi innowacjami w dziedzinie elektryczności.
Jak działa ogniwo galwaniczne i co je wyróżnia?
Ogniwo galwaniczne działa na zasadzie przekształcania energii chemicznej w energię elektryczną. Główne elementy ogniwa to dwa różne metale oraz elektrolit, który je otacza. Kiedy metale są zanurzone w elektrolicie, zachodzi reakcja chemiczna, która prowadzi do przepływu elektronów z jednego metalu do drugiego. To właśnie ten przepływ elektronów generuje prąd elektryczny, który można wykorzystać do zasilania różnych urządzeń.
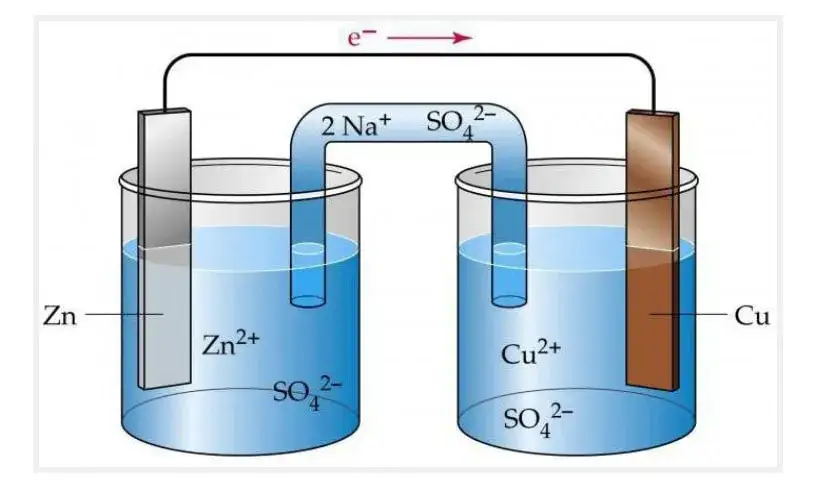
W skład ogniwa galwanicznego wchodzą dwa elektrod: anoda i katoda. Anoda to elektroda, na której zachodzi utlenianie, a katoda to miejsce, gdzie zachodzi redukcja. W zależności od użytych metali i rodzaju elektrolitu, różne ogniwa mogą mieć różne właściwości i zastosowania. Na przykład, ogniwo Daniella wykorzystuje cynk i miedź jako elektrody, co czyni je popularnym w zastosowaniach edukacyjnych oraz w prostych urządzeniach elektrycznych.
Zasada działania ogniwa galwanicznego w prostych słowach
Ogniwo galwaniczne działa na zasadzie przekształcania energii chemicznej w energię elektryczną. Kiedy dwa różne metale są zanurzone w elektrolicie, zachodzi reakcja chemiczna, która powoduje przepływ elektronów z jednego metalu do drugiego. Ten przepływ elektronów generuje prąd elektryczny, który możemy wykorzystać w różnych urządzeniach. W skrócie, ogniwo galwaniczne to prosty sposób na wytwarzanie energii elektrycznej z reakcji chemicznych.
W ogniwie galwanicznym kluczowe są dwa elementy: anoda i katoda. Anoda to elektroda, na której zachodzi utlenianie, a katoda to miejsce, gdzie zachodzi redukcja. Dzięki temu, że metale mają różne potencjały elektrochemiczne, możliwe jest generowanie prądu. To właśnie ta zasada działania sprawia, że ogniwa galwaniczne są tak ważne w technologii elektrycznej.
Kluczowe elementy ogniwa galwanicznego: metale i elektrolity
Ogniwa galwaniczne składają się z dwóch głównych komponentów: metali oraz elektrolitów. Najczęściej używane metale to cynk, miedź i ołów, a ich wybór wpływa na wydajność ogniwa. Cynk jest często stosowany jako anoda, ponieważ łatwo oddaje elektrony, podczas gdy miedź służy jako katoda, przyjmując te elektrony. Elektrolity, takie jak kwas siarkowy czy sól, są substancjami, które przewodzą prąd elektryczny i umożliwiają reakcje chemiczne między metalami.
Rola elektrolitu jest kluczowa, ponieważ to on umożliwia przepływ jonów, co z kolei pozwala na generowanie prądu. Bez odpowiedniego elektrolitu, ogniwo galwaniczne nie mogłoby funkcjonować. Dlatego zarówno wybór metali, jak i typ elektrolitu mają istotny wpływ na efektywność i zastosowanie ogniwa galwanicznego.
| Typ ogniwa | Materiały | Zastosowanie |
|---|---|---|
| Ogniwo Daniella | Cynk (anoda), Miedź (katoda), Kwas siarkowy (elektrolit) | Używane w prostych urządzeniach elektrycznych |
| Ogniwo Leclanché | Cynk (anoda), Węgiel (katoda), Roztwór amoniaku (elektrolit) | Stosowane w bateriach do zabawek i latarkach |
| Ogniwo alkaliczne | Cynk (anoda), Mangan (katoda), Kwas alkaliczny (elektrolit) | Wykorzystywane w bateriach do urządzeń domowych |
Jak wynalazek ogniwa galwanicznego wpłynął na świat?
Wynalazek ogniwa galwanicznego, stworzony przez Alessandra Voltę, zainicjował prawdziwą rewolucję technologiczną. Jego odkrycie umożliwiło przekształcanie energii chemicznej w elektryczną, co otworzyło drzwi do rozwoju wielu nowoczesnych technologii. Ogniwa galwaniczne stały się fundamentem dla późniejszych innowacji, takich jak baterie, które zrewolucjonizowały sposób, w jaki przechowujemy i wykorzystujemy energię. Dzięki nim możliwe stało się zasilanie urządzeń elektronicznych, co miało ogromny wpływ na codzienne życie ludzi.
Wpływ ogniwa galwanicznego na naukę i przemysł był ogromny. Dzięki niemu rozpoczęto szereg badań nad elektrycznością, co przyczyniło się do rozwoju teorii elektromagnetyzmu i technologii elektrycznej. Przemysł elektryczny zyskał na znaczeniu, a wynalazki takie jak telefony, lampy elektryczne i komputery stały się rzeczywistością. Ogniwa galwaniczne nie tylko zmieniły oblicze nauki, ale także wpłynęły na rozwój przemysłu, co z kolei przyczyniło się do postępu cywilizacyjnego.
Rewolucja w technologii: od ogniwa galwanicznego do baterii
Ogniwo galwaniczne stanowiło pierwszy krok w kierunku rozwoju nowoczesnych baterii. W miarę jak technologia się rozwijała, naukowcy zaczęli eksperymentować z różnymi materiałami, co doprowadziło do powstania bardziej zaawansowanych typów ogniw. Na przykład, ogniwa alkaliczne, które wykorzystują wodorotlenek potasu jako elektrolit, oferują znacznie większą pojemność i dłuższą żywotność niż tradycyjne ogniwa galwaniczne. Dzięki tym innowacjom, baterie stały się kluczowym elementem w technologii, zasilając wszystko, od prostych zabawek po skomplikowane urządzenia medyczne.
Współczesne baterie litowo-jonowe, które są używane w smartfonach i laptopach, również wywodzą się z początków technologii ogniw galwanicznych. Te nowoczesne rozwiązania pozwalają na przechowywanie dużych ilości energii w małych rozmiarach, co jest niezbędne w dzisiejszym świecie mobilnych technologii. Ewolucja od ogniwa galwanicznego do nowoczesnych baterii pokazuje, jak wynalazek Volt'a wpłynął na rozwój technologii, który trwa do dziś.Wpływ ogniwa galwanicznego na rozwój nauki i przemysłu
Wynalazek ogniwa galwanicznego miał ogromny wpływ na rozwój nauki i przemysłu. Dzięki możliwości przekształcania energii chemicznej w elektryczną, otworzył nowe perspektywy w badaniach nad elektrycznością. W rezultacie, naukowcy zaczęli prowadzić intensywne badania nad zjawiskami elektrycznymi, co przyczyniło się do rozwoju teorii elektromagnetyzmu. To z kolei doprowadziło do powstania innowacyjnych technologii, które zrewolucjonizowały przemysł, w tym produkcję energii, telekomunikację oraz elektronikę użytkową.
Ogniwo galwaniczne pozwoliło również na rozwój różnych zastosowań w przemyśle. Dzięki niemu możliwe stało się stworzenie nowoczesnych baterii, które zasilają wiele urządzeń codziennego użytku. Wprowadzenie ogniw galwanicznych przyczyniło się do powstania takich technologii jak ogniwa słoneczne, które są kluczowe w dziedzinie energii odnawialnej. W rezultacie, wynalazek Volt'a nie tylko zmienił oblicze nauki, ale także miał dalekosiężne konsekwencje dla całego przemysłu.
- Ogniwa alkaliczne - powszechnie stosowane w bateriach do zabawek i pilotów.
- Baterie litowo-jonowe - zasilają smartfony, laptopy i pojazdy elektryczne.
- Ogniwa słoneczne - wykorzystują energię słoneczną do produkcji energii elektrycznej.
- Ogniwa paliwowe - stosowane w pojazdach oraz systemach zasilania awaryjnego.
- Ogniwa niklowo-wodorkowe - używane w urządzeniach elektronicznych i narzędziach elektrycznych.
Przyszłość technologii ogniw galwanicznych w zrównoważonym rozwoju
W miarę jak świat staje przed wyzwaniami związanymi ze zmianami klimatycznymi, technologia ogniw galwanicznych zyskuje nowe znaczenie w kontekście zrównoważonego rozwoju. Wykorzystanie ogniw galwanicznych w systemach magazynowania energii odnawialnej, takich jak energia słoneczna i wiatrowa, staje się kluczowe dla efektywnego zarządzania energią. Dzięki nowoczesnym technologiom, takim jak ogniwa paliwowe i ogniwa sodowo-jonowe, możliwe jest nie tylko zwiększenie efektywności energetycznej, ale także zmniejszenie śladu węglowego w produkcji energii.
Inwestycje w badania i rozwój w dziedzinie nowoczesnych baterii oraz ogniw galwanicznych mogą przyczynić się do powstania bardziej ekologicznych rozwiązań. Na przykład, rozwój ogniw galwanicznych wykorzystujących materiały biodegradowalne lub recyklingowane może zrewolucjonizować sposób, w jaki podchodzimy do produkcji energii. W przyszłości, integracja ogniw galwanicznych z systemami inteligentnych sieci energetycznych (smart grids) może prowadzić do bardziej zrównoważonego i efektywnego zarządzania zasobami energetycznymi na całym świecie.


